
精硕生物:新冠病毒抗原检测试剂取得医疗器械注册证
4月20日,河北精硕生物科技有限公司的新型冠状病毒(2019-nCOV)抗原检测试剂盒(乳胶法)取得国家药监局颁发的《医疗器械注册证》,正式获批上市。这是石家庄市首个新冠抗原检测试剂获批上市。
据资深业内人士透露,迈瑞成为河北精硕生物科技有限公司总代理,正式入局新冠抗原检测。
精硕生物新型冠状病毒(2019-nCoV)抗原检测试剂盒(乳胶法)是对鼻拭子样本中新型冠状病毒抗原的检测,可用于体外定性检测新冠病毒N抗原。该试剂盒操作简便、快速,15分钟可获得检测结果,并有多种规格试剂,灵活应用,随到随检,对检测环境要求低。
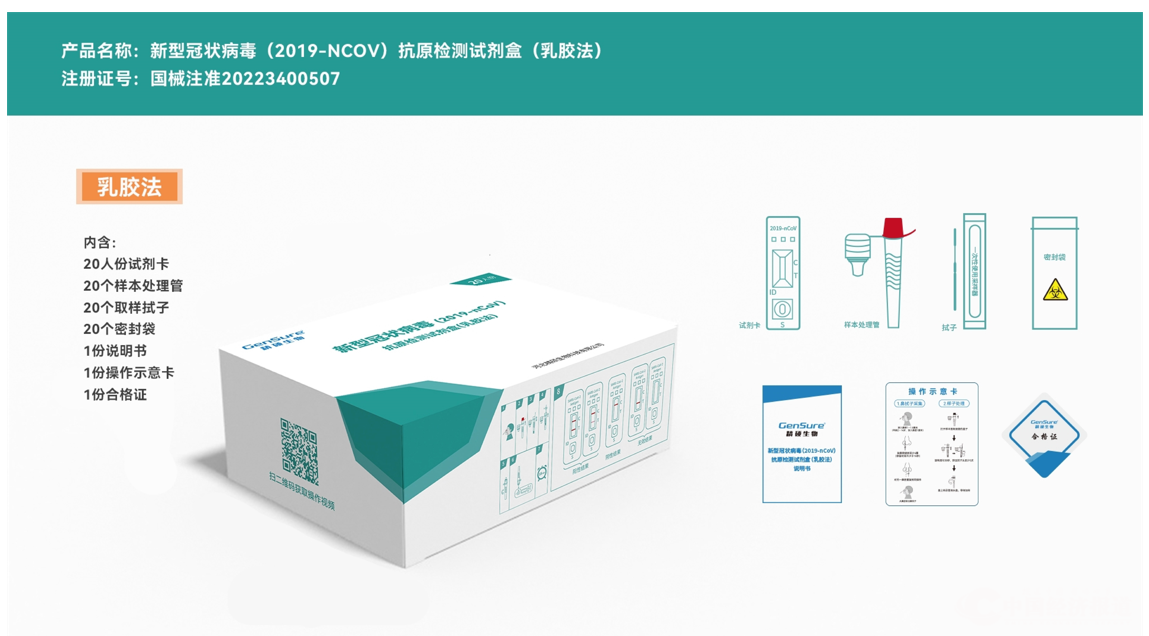
新冠病毒抗原检测试剂是精硕生物的核心产品之一。该产品于2020年8月份取得了欧盟CE证书,10月份进入了商务部防疫物资出口白名单。新冠病毒检测试剂项目被评为“河北省科技进步二等奖”,公司“新冠病毒N-S优势表位融合蛋白、制备方法、应用,及表达蛋白、微生物、应用”项目获中国新冠病毒检测领域首个专利。2021年以来,精硕生物新冠抗原检测试剂在欧盟、东南亚、俄罗斯、以色列等18个国家完成了注册并实现销售。

据了解,按照《新冠病毒抗原检测应用方案(试行)》的相关要求,可用于以下三类人员的检测:到基层医疗卫生机构就诊,伴有呼吸道、发热等症状且出现症状5天以内的人员;隔离观察人员,包括居家隔离观察、密接和次密接、入境隔离观察、封控区和管控区的人员;有抗原自我检测需求的社区居民。以上人员在使用新型冠状病毒抗原检测试剂时应遵循《新冠病毒抗原检测应用方案(试行)》等国家的相关管理要求。
精硕生物表示,公司新型冠状病毒(2019-nCoV)抗原检测试剂盒在国内获批上市,既丰富了产品种类,又增强了综合实力,还有助于提升公司在相关领域的竞争力,不仅对其销售及国内业务拓展具有积极的作用,还可以更好地为我国新冠疫情防控工作贡献力量。
来源:精硕生物官网、医业观察
























